Indice dei contenuti
Un orteil amputato che ricrescon nei topi grazie a due proteine: è il risultato ottenuto da un gruppo della Texas A&M University guidato dal biologo Ken Muneoka, pubblicato su Nature Communications. Negli animali trattati sono riapparsi ossa, tendini, legamenti e perfino strutture articolari, costruiti a partire dalle sole cellule presenti nel sito della ferita. Una capacità che fino a oggi sembrava riservata a creature come la salamandra e l’axolotl.
La trappola della cicatrizzazione
Quando un mammifero subisce una lesione grave o un’amputazione, il corpo risponde in emergenza inviando un esercito di fibroblasti, cellule incaricate di chiudere la breccia formando tessuto cicatriziale. È una tattica di sopravvivenza efficace per fermare un’emorragia potenzialmente letale, ma rappresenta anche un muro invalicabile: una volta che la cicatrice si è formata, l’arto non può più ricrescere.
È qui che si gioca la partita evolutiva tra noi e gli anfibi capaci di rigenerare. Loro non cicatrizzano nello stesso modo, noi sì, e questa scelta biologica privilegia la chiusura rapida rispetto alla ricostruzione completa. Il gruppo texano ha dovuto quindi “dirottare” il comportamento dei fibroblasti per ottenere un risultato diverso.
Due proteine, due ordini precisi
Il primo segnale chimico somministrato è stato FGF2, il fattore di crescita dei fibroblasti 2. Applicato sulla ferita, ha riprogrammato le cellule in piena attività, impedendo loro di cicatrizzare e mantenendole in uno stato temporaneo e ricettivo. Si è formato così quello che i biologi chiamano blastema: un germoglio di cellule malleabili, una sorta di pagina bianca cellulare in attesa di istruzioni di costruzione. Nei mammiferi questo bourgeon non compare spontaneamente dopo un’amputazione, ed è proprio la sua assenza a spiegare la nostra incapacità rigenerativa.
Una volta ottenuto artificialmente il blastema, i ricercatori hanno applicato una seconda proteina, la BMP2 (proteina morfogenetica ossea 2). Se il primo segnale forniva la materia prima, il secondo ha agito come architetto del cantiere. Ricevendo questa istruzione, il blastema ha iniziato a ricostruire metodicamente gli elementi mancanti.
Cosa è ricresciuto davvero
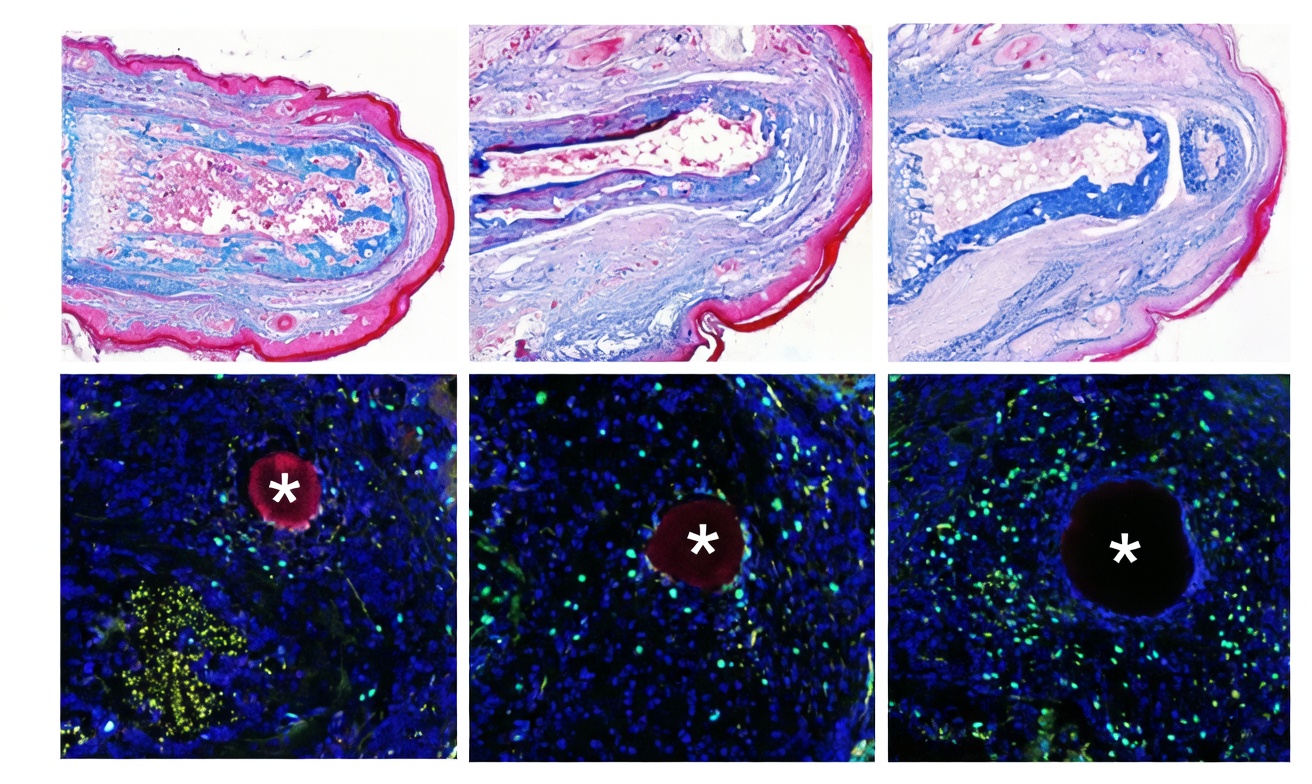
Nei test sulle zampe dei topi sono ricomparsi ossa, tendini, legamenti e strutture articolari dell’orteil amputato. Le nuove dita non erano perfette: talvolta di dimensioni imprecise o leggermente deformate. L’essenziale, però, c’era: l’anatomia complessa di una falange con le sue componenti era stata effettivamente ricreata partendo da una superficie di amputazione che, in condizioni normali, si sarebbe limitata a chiudersi.
L’aspetto più sorprendente di questo esperimento è la sua semplicità biologica. Le strategie attualmente esplorate dalla medicina rigenerativa prevedono spesso di prelevare cellule staminali, manipolarle in laboratorio e reiniettarle nel paziente. Qui non c’è nulla di tutto questo: i ricercatori si sono affidati esclusivamente alle cellule già presenti sul sito della ferita, limitandosi a fornire i segnali giusti al momento giusto.
Un potenziale dormiente
L’interpretazione più suggestiva è che il nostro organismo conservi, almeno in parte, le istruzioni genetiche necessarie a rigenerare un arto. Non gli mancherebbero gli strumenti, ma la sequenza di comandi corretta. La cicatrizzazione interverrebbe troppo in fretta, bloccando una procedura che, in teoria, le cellule saprebbero ancora eseguire. Una logica che ricorda quella di altri programmi biologici latenti che condividiamo con specie molto diverse da noi, e che attendono solo il segnale giusto per attivarsi.
Questa lettura cambia la prospettiva della medicina rigenerativa. Invece di costruire tessuti dall’esterno o coltivare organi in laboratorio, si tratterebbe di riattivare un programma latente, fornendo ai fibroblasti l’ordine di non fare ciò che fanno di default.
Quanto siamo lontani dall’applicazione umana
Le prove cliniche sull’uomo restano lontane. Una zampa di topo e un arto umano hanno scale, vascolarizzazioni e tempistiche di sviluppo molto diverse, e una falange è ben più semplice di una mano o di una gamba completa. Servirà capire se il meccanismo funziona su strutture più voluminose e in tessuti che non si limitano a un’estremità.
L’impatto a breve termine potrebbe comunque essere notevole. Le due proteine usate, BMP2 e FGF2, sono già autorizzate o in fase avanzata di autorizzazione per la chirurgia ricostruttiva. Questo significa che il loro uso combinato secondo il protocollo texano potrebbe entrare relativamente presto in sperimentazione per applicazioni più modeste: trattamento di ferite complesse, riduzione delle cicatrici definitive, miglioramento della guarigione di lesioni che oggi lasciano deficit funzionali permanenti. Non un arto nuovo, ma una guarigione qualitativamente diversa.