Nel 2008, un bambino belga di circa dieci anni con anemia falciforme si fece asportare e congelare un testicolo prima di affrontare la chemioterapia. Diciassette anni dopo, frammenti di quel tessuto immaturo sono tornati nel suo corpo e oggi producono spermatozoi maturi e mobili. Si tratta del primo caso al mondo documentato di ripristino della spermatogenesi a partire da tessuto testicolare prelevato nell'infanzia, condotto dall'University Hospital Brussels e dalla Vrije Universiteit Brussel.
Il problema che questa procedura cerca di risolvere è ben noto in oncologia pediatrica. Circa un terzo degli uomini sottoposti da bambini a trattamenti gonadotossici come radioterapia o chemioterapia risulta azoospermico dopo la pubertà: il loro eiaculato non contiene spermatozoi vitali. Per gli adulti la soluzione esiste da decenni e si chiama crioconservazione del seme, ma prima della pubertà i testicoli non producono ancora spermatozoi maturi, quindi quella strada è preclusa.
La biologia, però, offre una porta laterale. Anche nei testicoli prepuberi sono presenti le spermatogonial stem cells (SSC), cellule staminali che in età adulta darebbero origine agli spermatozoi. Congelare il tessuto che le contiene significa mettere in pausa quel potenziale. Nel 2002 l'ospedale universitario di Bruxelles è stato il primo al mondo a introdurre la pratica della crioconservazione di tessuto testicolare immaturo a scopo di fertilità futura. Da allora oltre 3.000 bambini nel mondo hanno banca di tessuto, in attesa che la ricerca dimostrasse se quel materiale potesse davvero essere riutilizzato.
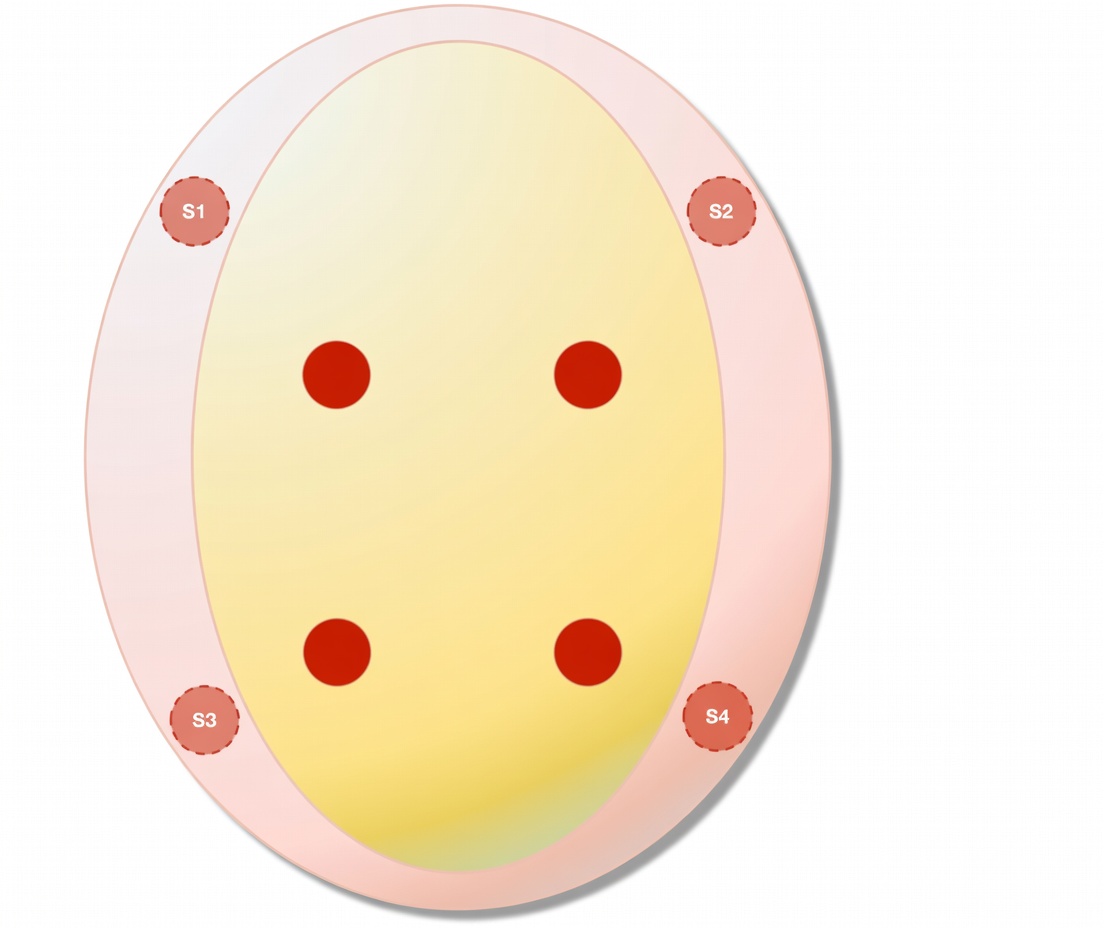
Il paziente belga è tornato in clinica nel 2022 chiedendo di diventare padre. L'analisi del testicolo rimasto ha confermato l'assenza di spermatozoi vitali. Nel 2025, all'interno di una sperimentazione clinica, i chirurghi hanno scongelato il tessuto conservato nel 2008 e impiantato otto innesti: quattro all'interno del testicolo residuo e quattro nello scroto. A distanza di un anno, alcuni di questi frammenti producono spermatozoi maturi e mobili, nonostante il campione di partenza contenesse, secondo gli autori, un numero "eccezionalmente basso" di SSC.
Il risultato ha però limiti precisi che vale la pena spiegare. Solo le porzioni di testicolo in cui sono stati collocati gli innesti contengono spermatozoi vitali, e queste aree non sono collegate al dotto deferente. In pratica, gli spermatozoi prodotti non raggiungono il liquido seminale durante l'eiaculazione. Per ottenere una gravidanza il paziente dovrà ricorrere a tecniche di procreazione assistita, con prelievo diretto dei gameti e fecondazione in laboratorio.
Rod Mitchell, endocrinologo pediatrico dell'Università di Edimburgo che conduce una sperimentazione analoga in Scozia, ha commentato il caso al Guardian: "Se congeli il tessuto e mantieni le cellule vive, allora dovrebbero avere il potenziale. Stai rimettendo il tessuto nell'ambiente perfetto per stimolarlo. Scientificamente e biologicamente ha senso. In realtà, resta comunque sorprendente."
Restano almeno tre domande aperte che la comunità scientifica considera centrali:
- la durata degli innesti nel tempo, dato che studi su modelli animali suggeriscono una sopravvivenza relativamente breve dei frammenti trapiantati;
- la qualità genetica ed epigenetica degli spermatozoi prodotti dopo congelamento, scongelamento e reimpianto;
- la possibilità che da questi gameti nascano bambini sani, con sviluppo embrionale e gravidanze monitorabili nel lungo periodo.
Il case study, depositato su medRxiv, deve ancora superare la revisione tra pari, e un singolo paziente non basta per dichiarare consolidata la procedura. La specialista in fertilità Veerle Vloeberghs di Brussels IVF ha spiegato la posizione del gruppo dopo l'intervento del 2025: "Si tratta di un passo importante nella ricerca scientifica per preservare la fertilità dei bambini con cancro o altre malattie del sangue. La procedura è specificamente pensata per ripristinare la fertilità, ma in questo momento non possiamo garantire che avrà successo o che i pazienti potranno avere figli."
Il punto, però, è proprio questo: per migliaia di adulti che da bambini hanno congelato tessuto testicolare in attesa di una soluzione, fino a ieri esisteva solo una speranza teorica. Ora c'è un primo dato biologico concreto. I ricercatori belgi seguiranno il paziente nel suo percorso verso la genitorialità biologica, monitorando lo sviluppo embrionale, l'andamento di un'eventuale gravidanza e la salute a lungo termine di un eventuale figlio. Sarà quel passaggio, più del trapianto in sé, a stabilire se il banking di tessuto testicolare pediatrico, oggi praticato in decine di ospedali nel mondo, mantenga davvero la promessa per cui è nato vent'anni fa.