Indice dei contenuti
Un dito amputato a un topo è ricresciuto con ossa, tendini, legamenti e strutture articolari grazie a due proteine somministrate in sequenza. L’esperimento, condotto dal team guidato da Ken Muneoka della Texas A&M University e pubblicato nel 2026 su Nature Communications, non produce arti perfetti, ma dimostra che le cellule dei mammiferi conservano istruzioni regenerative finora considerate dormienti o assenti.
Il problema della cicatrice
Quando un mammifero subisce una ferita profonda, la risposta predefinita è la formazione di tessuto cicatriziale. I fibroblasti, cellule del tessuto connettivo, raggiungono il sito danneggiato e lo richiudono rapidamente. È una strategia efficace per fermare l’emorragia e prevenire infezioni, ma chiude anche la porta a qualsiasi possibilità di ricrescita. Una salamandra o un axolotl, nelle stesse condizioni, fanno qualcosa di radicalmente diverso: invece di sigillare la ferita con una cicatrice, formano una struttura cellulare temporanea chiamata blastema, una specie di cantiere biologico che ricostruisce l’arto pezzo per pezzo.
L’idea alla base dello studio texano è che i fibroblasti dei mammiferi, mentre sono attivi nel riparare il danno, si trovino in uno stato recettivo in cui possono essere riprogrammati. Il problema non sarebbe quindi l’assenza delle istruzioni, ma la mancanza del segnale giusto al momento giusto.
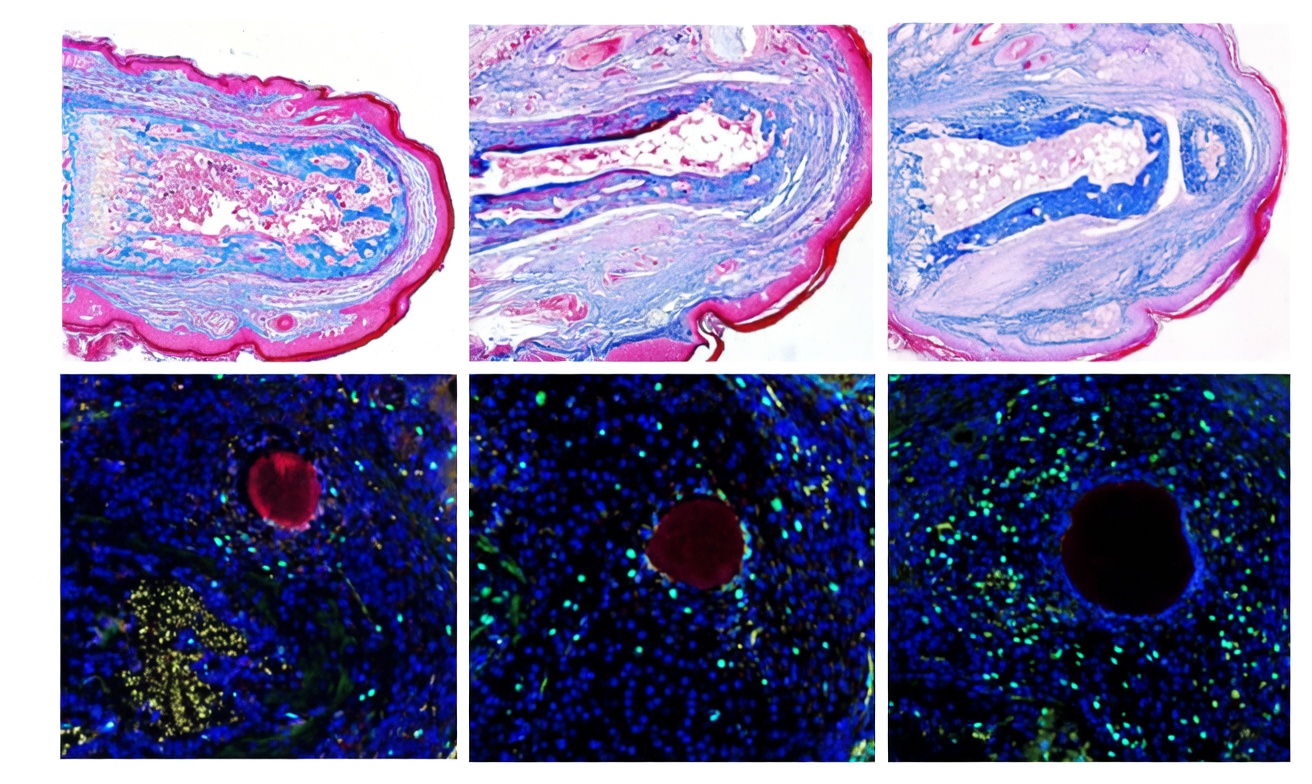
Due proteine, due fasi
Il protocollo si articola in due passaggi distinti. Nella prima fase i ricercatori applicano il fibroblast growth factor 2 (FGF2), una proteina che agisce sui fibroblasti dirottandoli dal loro destino cicatriziale verso uno stato simile a quello del blastema delle salamandre. Le cellule, in pratica, vengono convinte a non chiudere la ferita ma a prepararsi a costruire qualcosa di nuovo.
Nella seconda fase entra in gioco la bone morphogenetic protein 2 (BMP2), che fornisce alle cellule del blastema appena formato le istruzioni architettoniche per generare osso e tessuti connettivi. «È davvero un processo a due fasi», spiega Muneoka. «Prima allontani le cellule dalla cicatrizzazione, poi fornisci i segnali che dicono loro cosa costruire».
Sui topi che avevano perso un dito, la combinazione ha permesso di rigenerare ossa, tendini, legamenti e articolazioni. Le dita ricresciute erano talvolta più piccole del normale o leggermente deformate, ma tutti gli elementi strutturali essenziali erano presenti, e il risultato si è ripetuto in decine di tentativi.
Una strada diversa dalle staminali
L’approccio si distingue dal filone dominante della medicina rigenerativa, che punta sull’iniezione di cellule staminali capaci di differenziarsi in vari tipi di tessuto. Qui non si introducono cellule nuove: si lavora con quelle che già si trovano nel sito della ferita.
«Non devi prendere staminali e reinserirle», osserva Muneoka. «Sono già lì, devi solo imparare a farle comportare come vuoi». Un lavoro precedente dello stesso laboratorio aveva ottenuto rigenerazioni parziali usando solo BMP2, senza la formazione del blastema. L’aggiunta di FGF2 nella nuova ricerca segna la differenza: senza il primo passaggio, le cellule non vengono mai riprogrammate e la ricostruzione resta incompleta.
Cosa potrebbe arrivare in clinica
Il salto verso l’uomo richiede ancora molto lavoro, in particolare un’analisi più dettagliata dei meccanismi di ricrescita e la capacità di produrre arti che corrispondano davvero a quelli persi. Ci sono però due elementi che giocano a favore di possibili applicazioni nei prossimi anni:
- BMP2 è già approvata per l’uso in chirurgia ricostruttiva
- FGF2 sta seguendo un percorso simile verso l’approvazione clinica
Anche senza arrivare alla rigenerazione completa, la combinazione delle due proteine potrebbe migliorare la riparazione delle ferite e ridurre la formazione di cicatrici, due obiettivi clinici concreti che non richiedono di replicare l’impresa degli axolotl.
Il co-autore Larry Suva, fisiologo veterinario, sottolinea il cambio di prospettiva: «Una volta che dimostri che la rigenerazione può essere attivata, si apre la porta a domande completamente nuove». La questione di fondo, del resto, è antica. «Perché alcuni animali possono rigenerarsi e altri, in particolare gli esseri umani, non possono, è una grande domanda che si pone da Aristotele in poi», ricorda Muneoka. «Ho passato la mia carriera cercando di capirlo».
I topi non sono uomini, e un dito non è un braccio. Ma l’esperimento del Texas A&M suggerisce che la differenza tra una cicatrice e un arto rigenerato potrebbe non risiedere nel patrimonio genetico, quanto nella sequenza di segnali che le cellule ricevono nelle ore successive a una ferita.